Dystrofia mięśniowa Duchenne’a (DMD) to ciężka choroba genetyczna spowodowana brakiem dystrofiny, prowadząca do postępującego osłabienia mięśni. W przebiegu schorzenia kluczową rolę odgrywa dysfunkcja procesów usuwania uszkodzonych organelli, takich jak autofagia oraz specyficzna dla mitochondriów mitofagia. W niniejszym opracowaniu przeanalizowano wpływ oksygenazy hemowej-1 (HO-1) na te procesy w modelu mysim DMD (myszy mdx).
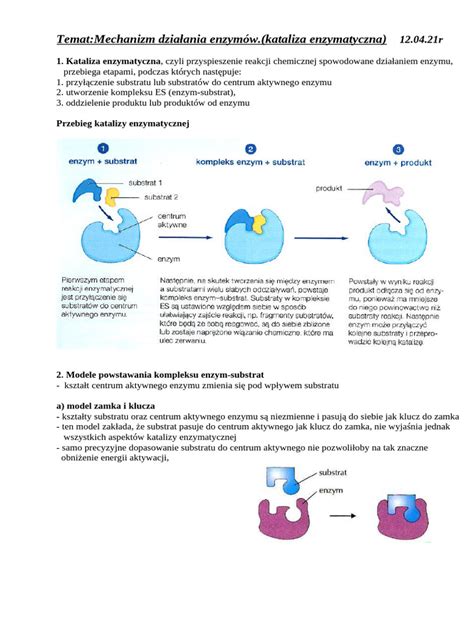
Autofagia i homeostaza mięśniowa w przebiegu DMD
Mięśnie szkieletowe charakteryzują się wysoką aktywnością metaboliczną i ciągłym narażeniem na stres mechaniczny oraz oksydacyjny. W zdrowym organizmie autofagia jest niezbędna dla prawidłowego funkcjonowania i naprawy tkanki mięśniowej. W dystrofii mięśniowej Duchenne’a dochodzi jednak do głębokiej dysregulacji tych procesów:
- Niewystarczająca autofagia: Prowadzi do gromadzenia się uszkodzonych białek i organelli.
- Nadmierny strumień autofagii: Może degradować ważne cząsteczki niezbędne dla integralności komórki.
Zaburzenia te, w połączeniu z dysfunkcją mitochondriów oraz zwiększoną produkcją reaktywnych form tlenu (ROS), znacząco przyczyniają się do postępu choroby.
Mitochondria
Rola oksygenazy hemowej-1 (HO-1)
Oksygenaza hemowa-1 (kodowana przez gen Hmox1) jest enzymem cytoprotekcyjnym, który poprzez degradację hemu generuje produkty o właściwościach przeciwzapalnych. W kontekście DMD rozważano HO-1 jako potencjalny cel terapeutyczny, mający na celu łagodzenie stresu oksydacyjnego.
Wyniki badań nad myszami mdx i mdx/Hmox1-/-
W badaniach przeprowadzonych na 6-tygodniowych myszach mdx oraz myszach z podwójnym nokautem (brak dystrofiny i HO-1) zaobserwowano następujące zależności:
| Parametr | Obserwacja w grupie mdx |
|---|---|
| Poziom mRNA (Bnip3, Pink1, Becn1) | Obniżony w mięśniu brzuchatym łydki |
| Siła mięśniowa | Spadek w porównaniu do grupy kontrolnej |
| Poziom LC3-II/LC3-I | Wzrost (sugerujący aktywność na poziomie potranslacyjnym) |
Choć brak Hmox1 wpłynął na skład krwi (procentowy udział limfocytów i monocytów) oraz poziom białek profibrotycznych, nie wykazano drastycznych różnic w poziomie markerów autofagii bezpośrednio wynikających z braku tego enzymu. Sugeruje to, że rola HO-1 w regulacji „samozjadania” komórek w DMD jest wysoce złożona i zależna od wieku zwierząt oraz typu mięśnia.
Wnioski z obserwacji zmian wiekowych
W badaniach przeprowadzonych na 12-tygodniowych myszach zaobserwowano odmienne wzorce ekspresji genów. Podczas gdy ekspresja Pink1 i Sqstm1 była obniżona, odnotowano zwiększoną aktywność genów Atg5, Atg7 oraz Lamp1. Zmiany te potwierdzają, że mechanizmy autofagii w dystrofii podlegają dynamicznym zmianom w czasie, co wymaga dalszych badań nad terapeutycznym wykorzystaniem nadprodukcji HO-1.